KEYTRUDA® pour le traitement néoadjuvant et adjuvant du CSTN de stade précoce à haut risque
-
EXPLOREZ KEYTRUDA® dans l’étude KEYNOTE-522 menée chez des patients venant de recevoir un diagnostic de CSTN de stade précoce à haut risque n’ayant jamais été traité.
Étude KEYNOTE-522 : Étude multicentrique, avec répartition aléatoire, à double insu et contrôlée, menée sur les traitements néoadjuvant et adjuvant des patients atteints d’un CSTN de stade précoce
Aperçu de l’étude
KEYNOTE-522 était une étude multicentrique, avec répartition aléatoire (2:1), à double insu et contrôlée par placebo, visant à évaluer l’efficacité et l’innocuité de KEYTRUDA® (pembrolizumab) comme traitement néoadjuvant, en association avec une chimiothérapie (le carboplatine et le paclitaxel, suivis de la doxorubicine en association avec le cyclophosphamide [AC] ou l’épirubicine en association avec le cyclophosphamide [EC]), puis comme traitement adjuvant, en monothérapie, après la chirurgie chez des patients qui ont récemment reçu un diagnostic de CSTN de stade précoce à haut risque n’ayant jamais été traité (N = 1 174)
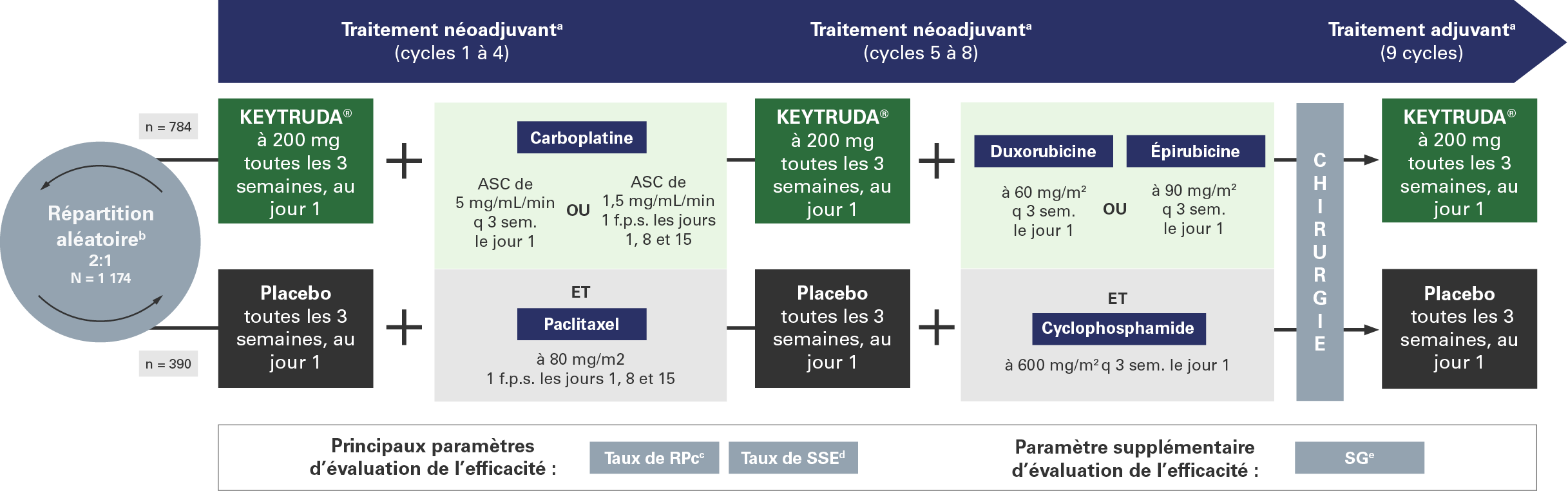
Critères d’admissibilité
- Cas nouvellement diagnostiqués de CSTN de stade précoce à haut risque n’ayant jamais été traité
- Taille de la tumeur > 1 cm mais ≤ 2 cm de diamètre avec atteinte ganglionnaire ou taille de la tumeur > 2 cm de diamètre, avec ou sans atteinte ganglionnaire
- Inscription peu importe l’expression du PD-L1
Paramètres d’évaluation principaux :
- Réponse pathologique complète (RPc), définie comme l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques (ypT0/Tis ypN0) et évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
- Survie sans événement (SSE), définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
Paramètres d’évaluation secondaires :
- Survie globale (SG)
ASC = aire sous la courbe; SSE = survie sans événement; SG = survie globale; RPc = réponse pathologique complète; CSTN = cancer du sein triple négatif; ypT0/Tis ypN0 = absence de cancer infiltrant dans le sein et les ganglions lymphatiques.
a Tous les médicaments à l’étude ont été administrés par voie intraveineuse.
b Le traitement avec KEYTRUDA® ou le placebo s’est poursuivi jusqu’à la fin du traitement (17 cycles), jusqu’à une progression de la maladie empêchant la chirurgie définitive, jusqu’à une récidive de la maladie pendant la phase adjuvante ou jusqu’à l’apparition d’une toxicité intolérable.
cLa RPc (ypT0/Tis ypN0) était définie par l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques et était évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
d La SSE était définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
e Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).§ Le carboplatine et le paclitaxel, suivis de la doxorubicine ou de l’épirubicine en association avec le cyclophosphamide.
* D’après une analyse provisoire prédéterminée de la SSE (comparativement à un seuil de signification de 0,0052).
‡ Basée sur la méthode de Miettinen et Nurminen, stratifiée en fonction de l’envahissement ganglionnaire, de la taille de la tumeur et de la décision de l’investigateur d’utiliser le carboplatine.
† D’après une analyse de suivi portant sur l’ensemble de la population en intention de traiter (n = 1 174), la différence entre les taux de RPc était de 7,5
(IC à 95 % : 1,6 à 13,4).
¶ Basé sur le modèle de régression de Cox, avec la méthode de traitement des contraintes d’Efron et le traitement comme covariable stratifiée selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
# Basée sur le test logarithmique par rangs stratifié selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.ASC = aire sous la courbe; SSE = survie sans événement; SG = survie globale; RPc = réponse pathologique complète; CSTN = cancer du sein triple négatif; ypT0/Tis ypN0 = absence de cancer infiltrant dans le sein et les ganglions lymphatiques.
a Tous les médicaments à l’étude ont été administrés par voie intraveineuse.
b Le traitement avec KEYTRUDA® ou le placebo s’est poursuivi jusqu’à la fin du traitement (17 cycles), jusqu’à une progression de la maladie empêchant la chirurgie définitive, jusqu’à une récidive de la maladie pendant la phase adjuvante ou jusqu’à l’apparition d’une toxicité intolérable.
c La RPc (ypT0/Tis ypN0) était définie par l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques et était évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
d La SSE était définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
e Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).§ Le carboplatine et le paclitaxel, suivis de la doxorubicine ou de l’épirubicine en association avec le cyclophosphamide.
* D’après une analyse provisoire prédéterminée de la SSE (comparativement à un seuil de signification de 0,0052).
‡ Basée sur la méthode de Miettinen et Nurminen, stratifiée en fonction de l’envahissement ganglionnaire, de la taille de la tumeur et de la décision de l’investigateur d’utiliser le carboplatine.
† D’après une analyse de suivi portant sur l’ensemble de la population en intention de traiter (n = 1 174), la différence entre les taux de RPc était de 7,5
(IC à 95 % : 1,6 à 13,4).
¶ Basé sur le modèle de régression de Cox, avec la méthode de traitement des contraintes d’Efron et le traitement comme covariable stratifiée selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
# Basée sur le test logarithmique par rangs stratifié selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.Réponse pathologique complète
KEYTRUDA® comme traitement néoadjuvant, en association avec une chimiothérapie, et KEYTRUDA® comme traitement adjuvant ont montré une amélioration statistiquement significative de la RPc vs le placebo administré avec une chimiothérapie et le placebo
Les patients recevant KEYTRUDA® (pembrolizumab) en association avec une chimiothérapie§ étaient 13,6 % plus nombreux à obtenir une RPc que ceux recevant le placebo en association avec une chimiothérapie§ IC à 95 % : 5,4 à 21,8; p = 0,00055)*‡.
KEYTRUDA® + chimiothérapie/KEYTRUDA® (n=401/602)Placebo + chimiothérapie/placebo (n=201/602)Nombre de patients présentant une RPc (ypT0/Tis ypN0) *†260103Taux de RPc, en % (ypT0/Tis ypN0)*64,8 (IC à 95 % : 59,9 à 69,5)51,2 (IC à 95 % : 44,1 à 58,3)Différence estimée entre les traitements, en %†‡13,6 (IC à 95 % : 5,4 à 21,8); p = 0,00055Survie sans événement
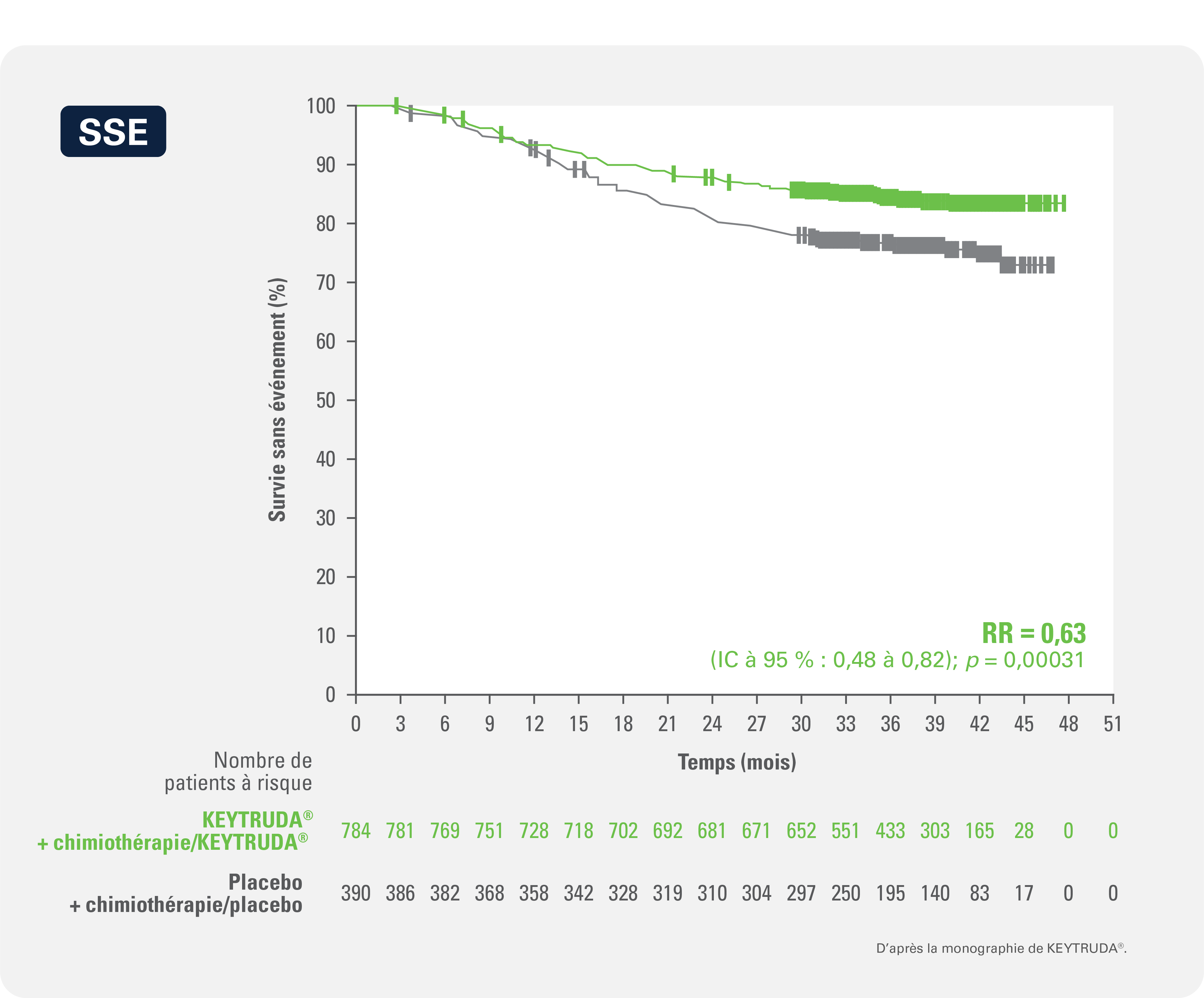
KEYTRUDA® comme traitement néoadjuvant, en association avec une chimiothérapie, et KEYTRUDA® comme traitement adjuvant ont montré une amélioration statistiquement significative de la SSE (RR : 0,63 [IC à 95 % : 0,48 à 0,82]; ¶ p = 0,00031#) vs le placebo administré avec une chimiothérapie et le placebo, et ont été associés à une réduction de 37 % du risque instantané d’événements
Courbe de Kaplan-Meier de la survie sans événement par groupe de traitement de l’étude KEYNOTE-522 (population en intention de traiter)
Survie globale
Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).
ASC = aire sous la courbe; SSE = survie sans événement; SG = survie globale; RPc = réponse pathologique complète; CSTN = cancer du sein triple négatif; ypT0/Tis ypN0 = absence de cancer infiltrant dans le sein et les ganglions lymphatiques.
a Tous les médicaments à l’étude ont été administrés par voie intraveineuse.
b Le traitement avec KEYTRUDA® ou le placebo s’est poursuivi jusqu’à la fin du traitement (17 cycles), jusqu’à une progression de la maladie empêchant la chirurgie définitive, jusqu’à une récidive de la maladie pendant la phase adjuvante ou jusqu’à l’apparition d’une toxicité intolérable.
c La RPc (ypT0/Tis ypN0) était définie par l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques et était évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
d La SSE était définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
e Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).
§ Le carboplatine et le paclitaxel, suivis de la doxorubicine ou de l’épirubicine en association avec le cyclophosphamide.
* D’après une analyse provisoire prédéterminée de la SSE (comparativement à un seuil de signification de 0,0052).
‡ Basée sur la méthode de Miettinen et Nurminen, stratifiée en fonction de l’envahissement ganglionnaire, de la taille de la tumeur et de la décision de l’investigateur d’utiliser le carboplatine.
† D’après une analyse de suivi portant sur l’ensemble de la population en intention de traiter (n = 1 174), la différence entre les taux de RPc était de 7,5
(IC à 95 % : 1,6 à 13,4).
¶ Basé sur le modèle de régression de Cox, avec la méthode de traitement des contraintes d’Efron et le traitement comme covariable stratifiée selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
# Basée sur le test logarithmique par rangs stratifié selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
ASC = aire sous la courbe; SSE = survie sans événement; SG = survie globale; RPc = réponse pathologique complète; CSTN = cancer du sein triple négatif; ypT0/Tis ypN0 = absence de cancer infiltrant dans le sein et les ganglions lymphatiques.
a Tous les médicaments à l’étude ont été administrés par voie intraveineuse.
b Le traitement avec KEYTRUDA® ou le placebo s’est poursuivi jusqu’à la fin du traitement (17 cycles), jusqu’à une progression de la maladie empêchant la chirurgie définitive, jusqu’à une récidive de la maladie pendant la phase adjuvante ou jusqu’à l’apparition d’une toxicité intolérable.
c La RPc (ypT0/Tis ypN0) était définie par l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques et était évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
d La SSE était définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
e Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).§ Le carboplatine et le paclitaxel, suivis de la doxorubicine ou de l’épirubicine en association avec le cyclophosphamide.
* D’après une analyse provisoire prédéterminée de la SSE (comparativement à un seuil de signification de 0,0052).
‡ Basée sur la méthode de Miettinen et Nurminen, stratifiée en fonction de l’envahissement ganglionnaire, de la taille de la tumeur et de la décision de l’investigateur d’utiliser le carboplatine.
† D’après une analyse de suivi portant sur l’ensemble de la population en intention de traiter (n = 1 174), la différence entre les taux de RPc était de 7,5
(IC à 95 % : 1,6 à 13,4).
¶ Basé sur le modèle de régression de Cox, avec la méthode de traitement des contraintes d’Efron et le traitement comme covariable stratifiée selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
# Basée sur le test logarithmique par rangs stratifié selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.Profil d’innocuité établi de KEYTRUDA® chez les patients atteints d’un CSTN de stade précoce à haut risque
Effets indésirables de grade 3 à 5 liés au traitement les plus fréquents (signalés chez ≥ 5 % des patients) :
D’après la monographie de KEYTRUDA®Effet indésirableKEYTRUDA® 200 mg toutes les 3 semaines + chimiothérapie*/KEYTRUDA® 200 mg toutes les 3 semaines
(n = 783)Placebo + chimiothérapie*/placebo
(n = 389)Neutropénie34,5 %33,4 %Diminution du nombre de neutrophiles18,6 %23,1 %Anémie18 %14,9 %Neutropénie fébrile17,8 %16 %Diminution du nombre de leucocytes7,7 %5,2 %Augmentation du taux d’alanine aminotransférase5,5 %2,3 %- Des effets indésirables mortels sont survenus, indépendamment du lien de causalité, chez 0,9 % des patients recevant KEYTRUDA® comme traitement néoadjuvant, en association avec une chimiothérapie, et comme traitement adjuvant par la suite, en monothérapie, après la chirurgie, y compris un cas chacun d’encéphalite auto-immune, de pneumonie, de pneumonite, d’embolie pulmonaire, de septicémie associée au syndrome de dysfonctionnement d’organes multiples, d’infarctus du myocarde et de choc. Enfin, un patient a trouvé la mort pour une raison inconnue.
- Des effets indésirables graves liés au traitement se sont manifestés chez 34 % des patients recevant KEYTRUDA®.
- Le traitement avec KEYTRUDA® a été abandonné en raison d’effets indésirables liés au traitement chez 49 % des patients.
Effets indésirables liés au traitement, tous grades confondus (signalés chez ≥ 20 % des patients) :
D’après la monographie de KEYTRUDA®Effet indésirableKEYTRUDA® 200 mg toutes les 3 semaines + chimiothérapie*/KEYTRUDA® 200 mg toutes les 3 semaines
(n = 783)Placebo + chimiothérapie*/placebo
(n = 389)Nausées63,2 %63,0 %Alopécie60,2 %56,6 %Anémie54,8 %55,3 %Neutropénie46,9 %47,6 %Fatigue42,1 %38,8 %Diarrhée30,4 %25,2 %Augmentation du taux d’alanine aminotransférase26,1 %25,2 %Neuropathie périphérique19,7 %21,6 %Diminution de l’appétit19,5 %14,7 %ASC = aire sous la courbe; SSE = survie sans événement; SG = survie globale; RPc = réponse pathologique complète; CSTN = cancer du sein triple négatif; ypT0/Tis ypN0 = absence de cancer infiltrant dans le sein et les ganglions lymphatiques.
a Tous les médicaments à l’étude ont été administrés par voie intraveineuse.
b Le traitement avec KEYTRUDA® ou le placebo s’est poursuivi jusqu’à la fin du traitement (17 cycles), jusqu’à une progression de la maladie empêchant la chirurgie définitive, jusqu’à une récidive de la maladie pendant la phase adjuvante ou jusqu’à l’apparition d’une toxicité intolérable.
c La RPc (ypT0/Tis ypN0) était définie par l’absence de cancer infiltrant dans le sein et les ganglions lymphatiques et était évaluée par le pathologiste local, à l’insu, au moment de la chirurgie définitive.
d La SSE était définie comme le temps écoulé entre la répartition aléatoire et la survenue du premier événement parmi les suivants : progression de la maladie empêchant d’effectuer une chirurgie définitive, récidive locale ou distante, deuxième tumeur maligne primaire ou décès, quelle qu’en soit la cause.
e Au moment de l’analyse de la SSE, les données relatives à la SG n’étaient pas complètes (45 % du nombre d’événements requis pour l’analyse finale de la SG).§ Le carboplatine et le paclitaxel, suivis de la doxorubicine ou de l’épirubicine en association avec le cyclophosphamide.
* D’après une analyse provisoire prédéterminée de la SSE (comparativement à un seuil de signification de 0,0052).
‡ Basée sur la méthode de Miettinen et Nurminen, stratifiée en fonction de l’envahissement ganglionnaire, de la taille de la tumeur et de la décision de l’investigateur d’utiliser le carboplatine.
† D’après une analyse de suivi portant sur l’ensemble de la population en intention de traiter (n = 1 174), la différence entre les taux de RPc était de 7,5
(IC à 95 % : 1,6 à 13,4).
¶ Basé sur le modèle de régression de Cox, avec la méthode de traitement des contraintes d’Efron et le traitement comme covariable stratifiée selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
# Basée sur le test logarithmique par rangs stratifié selon l’envahissement ganglionnaire, la taille de la tumeur et la décision de l’investigateur d’utiliser le carboplatine.
KEYTRUDA® pour le traitement de première intention du CSTN non résécable, localement récidivant ou métastatique
-
EXPLOREZ KEYTRUDA® dans l’étude KEYNOTE-355 menée chez des patients atteints d’un CSTN non résécable, localement récidivant ou métastatique n’ayant reçu aucun traitement de chimiothérapie contre une maladie métastatique
Étude KEYNOTE-355 : Étude multicentrique, à double insu, contrôlée par placebo et avec répartition aléatoire visant à évaluer KEYTRUDA® dans le traitement du cancer du CSTN non résécable, localement récidivant ou métastatique
Aperçu de l’étude
Étude KEYNOTE-355 était une étude à répartition aléatoire et à double insu portant sur KEYTRUDA® en association avec une chimiothérapie vs l’association placebo + chimiothérapie menée chez des patients n’ayant jamais été traités et atteints d’un CSTN non résécable, localement récidivant ou métastatique sans égard au statut d’expression du PD-L1 de la tumeur ¶. Au total, 847 patients ont été répartis au hasard (selon un rapport 2:1) et les patients ont reçu KEYTRUDA® à raison de 200 mg par voie intraveineuse toutes les 3 semaines (n = 556) ou le placebo par voie intraveineuse toutes les 3 semaines (n = 281).
KEYTRUDA® est indiqué pour le traitement, en association avec une chimiothérapie, des adultes atteints d’un cancer du sein triple négatif (CSTN) non résécable, localement récidivant ou métastatique, qui n’ont jamais reçu de chimiothérapie pour traiter une maladie métastatique et dont les tumeurs expriment le PD-L1 (SCP ≥ 10), tel que déterminé par un test validé.
Groupes de traitement
KEYTRUDA® à raison de 200 mg au jour 1 de chaque cycle de 3 semaines, en association avec
le nab-paclitaxel à raison de 100 mg/m2 aux jours 1, 8 et 15 de chaque cycle de 28 jours, ou
le paclitaxel à raison de 90 mg/m2 aux jours 1, 8 et 15 de chaque cycle de 28 jours, ou
la gemcitabine à raison de 1 000 mg/m2 et le carboplatine à une ASC cible de 2 mg/mL/min aux jours 1 et 8 de chaque cycle de 21 jour
(n = 566; SCP ≥ 10 : n = 220)
Placebo au jour 1 de chaque cycle de 3 semaines, en association avec
le nab-paclitaxel à raison de 100 mg/m2 aux jours 1, 8 et 15 de chaque cycle de 28 jours, ou
le paclitaxel à raison de 90 mg/m2 aux jours 1, 8 et 15 de chaque cycle de 28 jours, ou
la gemcitabine à raison de 1 000 mg/m2 et le carboplatine à une ASC cible de 2 mg/mL/min aux jours 1 et 8 de chaque cycle de 21 jours
(n = 281; SCP ≥ 10 : n = 103)
Principaux critères d’admissibilité
- Âge ≥ 18 ans
- CSTN confirmé par un laboratoire central (selon les lignes directrices de l’ASCO / du CAP)
- ≥ 1 lésion mesurable conformément aux critères RECIST 1.1
- Échantillon d’une tumeur localement récidivante et inopérable ou métastatique
- Fin du traitement avec intention curative ≥ 6 mois avant la première récidive de la maladie
- Indice fonctionnel de l’ECOG : 0 ou 1
- Fonctionnement adéquat des organes
Principaux paramètres d’efficacité :
- Survie sans progression selon la version 1.1 des critères RECIST, obtenue au moyen d’une évaluation centralisée indépendante menée à l’insu, modifiée pour assurer le suivi d’au plus 10 lésions cibles et d’au plus 5 lésions cibles par organe chez les patients présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
- Survie globale chez les patients présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
Autres paramètres d’efficacité :
- Taux de réponse objective (TRO) chez les patients présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
- Durée de la réponse (DR) chez les patients présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
ASCO-CAP = American Society of Clinical Oncology – College of American Pathologists; IC = intervalle de confiance; SCP = score combiné positif; ECOG = Eastern Cooperative Oncology Group; RR = rapport de risque; CSTN = cancer du sein triple négatif; PD-L1 = ligand 1 de la mort cellulaire programmée; RECIST=Response Evaluation Criteria In Solid Tumors (critères d’évaluation de la réponse dans les tumeurs solides).
¶ En tout, 38 % des 847 patients présentaient une tumeur exprimant le PD-L1 avec un SCP ≥ 10
‡ Basé sur le modèle de régression de Cox.
Þ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,00411)
§ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,0113).
* Chimiothérapie : paclitaxel, nab-paclitaxel, ou gemcitabine et carboplatine.
# D’après l’analyse finale prédéterminée (date limite pour l’inclusion des données : 15 juin 2021).
† Fondés sur la version 1.1 des critères RECIST, obtenus au moyen d’une évaluation centralisée indépendante menée à l’insu..
** D’après une analyse provisoire prédéterminée (date limite pour l’inclusion des données : 11 décembre 2019).ASCO-CAP = American Society of Clinical Oncology – College of American Pathologists; IC = intervalle de confiance; SCP = score combiné positif; ECOG = Eastern Cooperative Oncology Group; RR = rapport de risque; CSTN = cancer du sein triple négatif; PD-L1 = ligand 1 de la mort cellulaire programmée; RECIST=Response Evaluation Criteria In Solid Tumors (critères d’évaluation de la réponse dans les tumeurs solides).
¶ En tout, 38 % des 847 patients présentaient une tumeur exprimant le PD-L1 avec un SCP ≥ 10
‡ Basé sur le modèle de régression de Cox.
Þ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,00411).
§ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,0113).
* Chimiothérapie : paclitaxel, nab-paclitaxel, ou gemcitabine et carboplatine.
# D’après l’analyse finale prédéterminée (date limite pour l’inclusion des données : 15 juin 2021).
† Fondés sur la version 1.1 des critères RECIST, obtenus au moyen d’une évaluation centralisée indépendante menée à l’insu.
** D’après une analyse provisoire prédéterminée (date limite pour l’inclusion des données : 11 décembre 2019).Survie sans progression
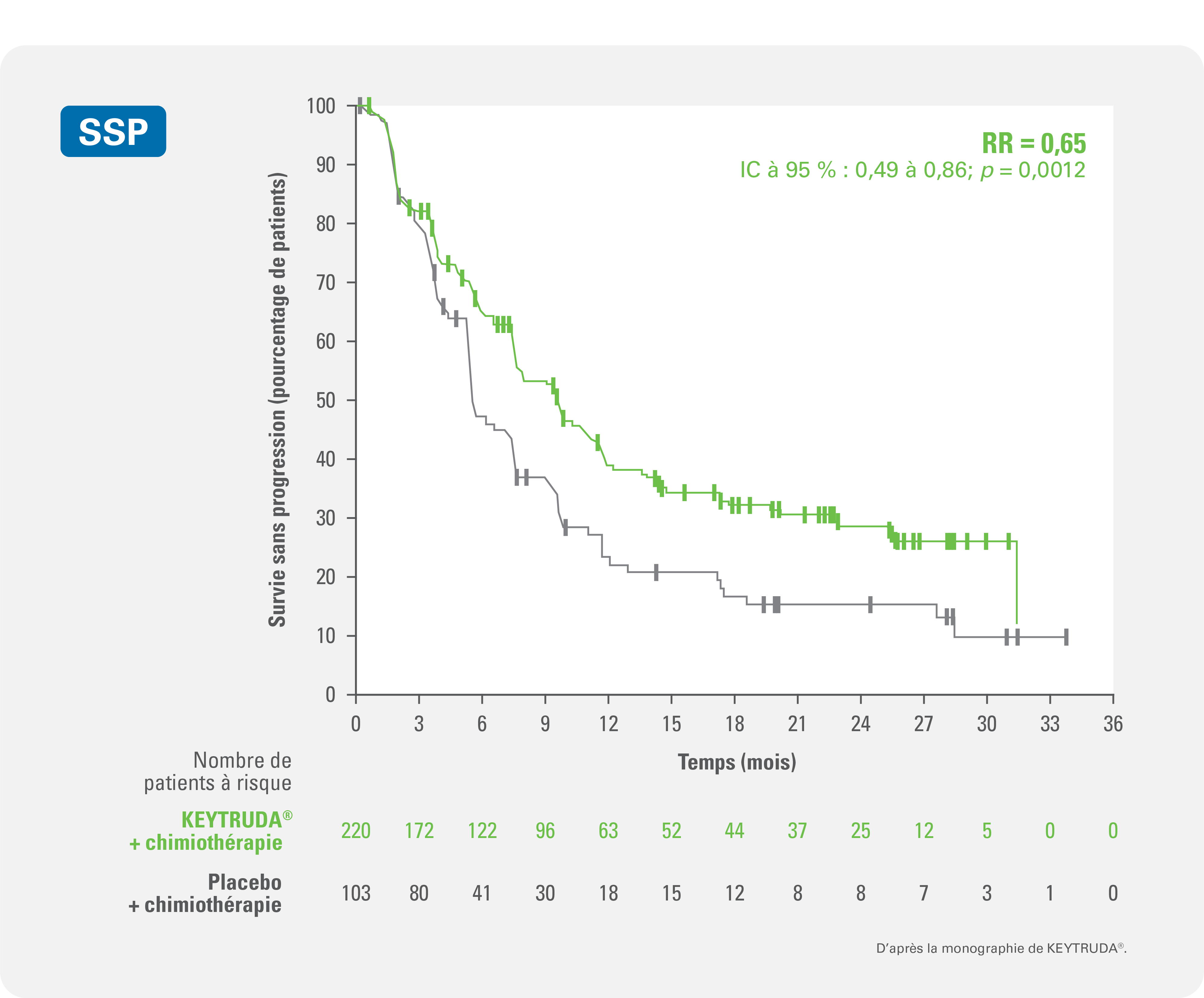
L’association KEYTRUDA® + chimiothérapie a entraîné une amélioration significative de la survie sans progression (SSP) vs l’association placebo + chimiothérapie
Réduction de 35 % du risque instantané de décès ou de progression de la maladie pour l’association KEYTRUDA® + chimiothérapie vs l’association placebo + chimiothérapie (RR‡ = 0,65; IC à 95 % : 0,49 à 0,86; pÞ,§ = 0,0012)
Courbe de Kaplan-Meier de la survie sans progression par groupe de traitement de l’étude KEYNOTE-355 (avec SCP ≥ 10)
Survie sans progression médiane
Survie sans progression médiane chez les patients atteints d’un cancer du sein triple négatif non résécable, localement récidivant ou métastatique et présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
SSP médiane en moisKEYTRUDA® + chimiothérapie*
(n=220)Placebo + chimiothérapie*
(n=103)9,7 mois
(IC à 95 % : 7,6 à 11,3)5,6 mois
(IC à 95 % : 5,3 à 7,5)Survie globale
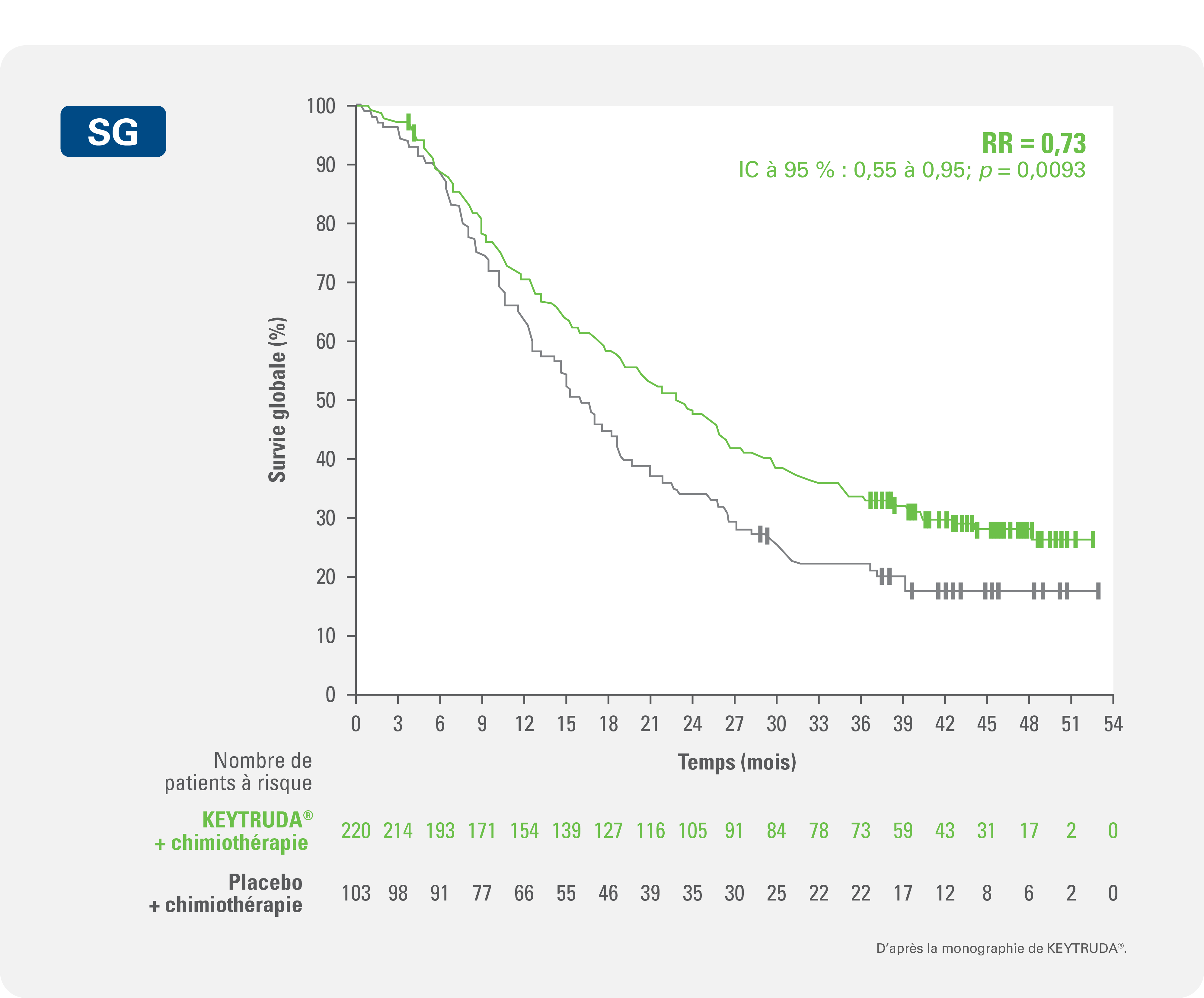
L’association KEYTRUDA® + chimiothérapie a entraîné une amélioration significative de la survie globale (SG) vs l’association placebo + chimiothérapie
Réduction de 27 % du risque instantané de décès ou de progression de la maladie pour l’association KEYTRUDA® + chimiothérapie vs l’association placebo + chimiothérapie (RR# = 0,73 (0,55 à 0,95); p§ = 0,0093)
Courbe de Kaplan-Meier de la survie globale par groupe de traitement de l’étude KEYNOTE-355 (avec SCP ≥ 10)
Taux de réponse objective
Taux de réponse objective chez les patients atteints d’un cancer du sein triple négatif non résécable, localement récidivant ou métastatique et présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10
TRO (IC à 95 %)KEYTRUDA® + chimiothérapie*
(n=220)Placebo + chimiothérapie*
(n=103)53 % (IC à 95 % : 46 à 59)41 % (IC à 95 % : 31 à 51)Durée de la réponse
Durée de la réponse, médiane en mois (intervalle) chez des patients atteints d’un CSTN non résécable, localement récidivant ou métastatique et présentant une tumeur exprimant le PD-L1 avec un SCP ≥ 10†**
KEYTRUDA® + chimiothérapie*
(n=220)Placebo + chimiothérapie*
(n=103)12,87,3ASCO-CAP = American Society of Clinical Oncology – College of American Pathologists; IC = intervalle de confiance; SCP = score combiné positif; ECOG = Eastern Cooperative Oncology Group; RR = rapport de risque; CSTN = cancer du sein triple négatif; PD-L1 = ligand 1 de la mort cellulaire programmée; RECIST=Response Evaluation Criteria In Solid Tumors (critères d’évaluation de la réponse dans les tumeurs solides).
¶ En tout, 38 % des 847 patients présentaient une tumeur exprimant le PD-L1 avec un SCP ≥ 10
‡ Basé sur le modèle de régression de Cox.
Þ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,00411)
§ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,0113).
* Chimiothérapie : paclitaxel, nab-paclitaxel, ou gemcitabine et carboplatine.
# D’après l’analyse finale prédéterminée (date limite pour l’inclusion des données : 15 juin 2021).
† Fondés sur la version 1.1 des critères RECIST, obtenus au moyen d’une évaluation centralisée indépendante menée à l’insu..
** D’après une analyse provisoire prédéterminée (date limite pour l’inclusion des données : 11 décembre 2019).ASCO-CAP = American Society of Clinical Oncology – College of American Pathologists; IC = intervalle de confiance; SCP = score combiné positif; ECOG = Eastern Cooperative Oncology Group; RR = rapport de risque; CSTN = cancer du sein triple négatif; PD-L1 = ligand 1 de la mort cellulaire programmée; RECIST=Response Evaluation Criteria In Solid Tumors (critères d’évaluation de la réponse dans les tumeurs solides).
¶ En tout, 38 % des 847 patients présentaient une tumeur exprimant le PD-L1 avec un SCP ≥ 10
‡ Basé sur le modèle de régression de Cox.
Þ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,00411).
§ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,0113).
* Chimiothérapie : paclitaxel, nab-paclitaxel, ou gemcitabine et carboplatine.
# D’après l’analyse finale prédéterminée (date limite pour l’inclusion des données : 15 juin 2021).
† Fondés sur la version 1.1 des critères RECIST, obtenus au moyen d’une évaluation centralisée indépendante menée à l’insu.
** D’après une analyse provisoire prédéterminée (date limite pour l’inclusion des données : 11 décembre 2019).Profil d’innocuité démontré pour le traitement du CSTN non résécable, localement récidivant ou métastatique
Effets indésirables liés au traitement de grades 3 à 5 les plus fréquents liés au traitement chez les patients traités avec KEYTRUDA® (signalés chez au moins 20 % des patients)
D’après la monographie de KEYTRUDA ®.Effet indésirableKEYTRUDA® + chimiothérapie (n=596)Placebo + chimiothérapie (n=281)Neutropénie29,229,9Diminution du nombre de neutrophiles17,311,0Anémie16,414,6Diminution du nombre de leucocytes10,210,3Thrombopénie9,911,1Leucopénie9,710,7Diminution du nombre de plaquettes6,04,3Augmentation du taux d’alanine aminotransférase5,74,6- KEYTRUDA® a été abandonné en raison d’effets indésirables liés au traitement chez 9,1 % des patients.
- Des effets indésirables mortels liés au traitement sont survenus chez 0,3 % des patients recevant KEYTRUDA® en association avec une chimiothérapie, y compris un cas chacun de pneumonie et d’atteinte rénale aiguë.
- Des effets indésirables graves liés au traitement sont survenus chez 17,6 % des patients traités avec KEYTRUDA® en association avec une chimiothérapie.
- KEYTRUDA® a été interrompu en raison d’effets indésirables liés au traitement chez 43 % des patients.
Effets indésirables liés au traitement les plus fréquents (signalés chez ≥ 20 % des patients), tous grades confondus, dans le groupe KEYTRUDA® + chimiothérapie vs le groupe placebo + chimiothérapie
D’après la monographie de KEYTRUDA®.Effet indésirableKEYTRUDA® + chimiothérapie (n=596)Placebo + chimiothérapie (n=281)Anémie48,845,9Neutropénie40,438,1Nausées38,440,9Alopécie33,133,5Fatigue27,529,5Diminution du nombre de neutrophiles22,126,3ASCO-CAP = American Society of Clinical Oncology – College of American Pathologists; IC = intervalle de confiance; SCP = score combiné positif; ECOG = Eastern Cooperative Oncology Group; RR = rapport de risque; CSTN = cancer du sein triple négatif; PD-L1 = ligand 1 de la mort cellulaire programmée; RECIST=Response Evaluation Criteria In Solid Tumors (critères d’évaluation de la réponse dans les tumeurs solides).
¶ En tout, 38 % des 847 patients présentaient une tumeur exprimant le PD-L1 avec un SCP ≥ 10
‡ Basé sur le modèle de régression de Cox.
Þ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,00411).
§ Valeur p unilatérale, calculée à l’aide du test logarithmique par rangs stratifié (comparativement à un seuil de signification de 0,0113).
* Chimiothérapie : paclitaxel, nab-paclitaxel, ou gemcitabine et carboplatine.
# D’après l’analyse finale prédéterminée (date limite pour l’inclusion des données : 15 juin 2021).
† Fondés sur la version 1.1 des critères RECIST, obtenus au moyen d’une évaluation centralisée indépendante menée à l’insu.
** D’après une analyse provisoire prédéterminée (date limite pour l’inclusion des données : 11 décembre 2019).
References
1. Monographie de KEYTRUDA®. Merck Canada Inc., 6 février 2024.
2. Schmid et al. Event-free Survival with Pembrolizumab in Early Triple-Negative Breast Cancer. N Eng J Medicine. 2022:386(6);556-567.
CA-OBR-00006

